La Administración de Alimentos y Medicamentos de Estados Unidos (FDA) ha dado luz verde a dos innovadoras terapias genéticas, Casgevy y Lyfgenia, diseñadas para abordar la anemia de células falciformes.
Este avance, impulsado por la tecnología revolucionaria de edición genética CRISPR, representa una esperanza tangible para aquellos que enfrentan los desafíos debilitantes de esta enfermedad hereditaria.
A continuación, exploraremos los detalles detrás de esta emocionante noticia y su significado en el campo de la medicina.
Antecedentes de las terapias genéticas
La anemia de células falciformes, un trastorno sanguíneo doloroso y potencialmente mortal, afecta a cerca de 100,000 personas en Estados Unidos, en su mayoría afroamericanos y en menor medida, hispanoamericanos.
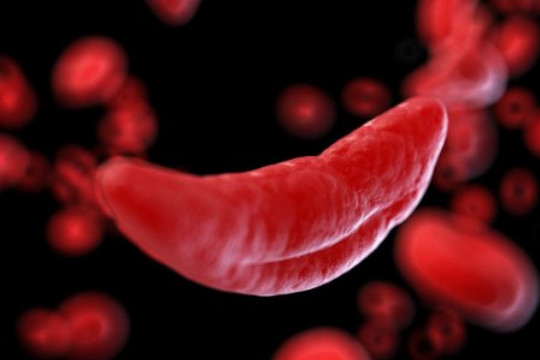
Los glóbulos rojos con forma de hoz característicos de esta enfermedad limitan el flujo sanguíneo, provocando dolor intenso y daño a los órganos.
En respuesta a esta necesidad médica insatisfecha, la FDA ha aprobado dos terapias genéticas pioneras: Casgevy y Lyfgenia.
Casgevy y Lyfgenia en beneficio de las terapias genéticas
Casgevy, desarrollado por Vertex Pharmaceuticals y CRISPR Therapeutics, marca un hito al ser el primer tratamiento aprobado por la FDA que utiliza la tecnología de edición genética CRISPR.
Esta herramienta innovadora, conocida como las «tijeras CRISPR,» fue reconocida con el Premio Nobel de Química en 2020 para las científicas Emmanuelle Charpentier y Jennifer Doudna.
Casgevy ofrece un enfoque específico y eficaz al modificar genéticamente las células madre sanguíneas del propio paciente.
En el caso de Lyfgenia, esta modalidad de terapia genética también ha obtenido la aprobación de la FDA. Esta terapia se basa en la modificación de las células madre sanguíneas del paciente y se administra como parte de un trasplante de células madre hematopoyéticas.
La eficacia de Lyfgenia se evaluó en un estudio multicéntrico de 24 meses, destacando su impacto positivo en la resolución de eventos vasooclusivos en pacientes con anemia de células falciformes.
Procedimiento de tratamiento y seguimiento a largo plazo
Ambos tratamientos siguen un proceso similar: recolección de células madre del propio paciente, seguido de acondicionamiento mieloablativo para eliminar células de la médula ósea.
Luego, las células modificadas se infunden en el paciente como parte del trasplante de células madre hematopoyéticas. La FDA subraya la importancia de seguir a los pacientes a largo plazo para evaluar la seguridad y eficacia de estos tratamientos innovadores.
La aprobación de Casgevy y Lyfgenia refleja el compromiso de la FDA con el desarrollo de tratamientos seguros y eficaces para condiciones de salud significativas.
Peter Marks, director del Centro de Evaluación e Investigación de Productos Biológicos de la FDA, enfatiza la importancia de las rigurosas evaluaciones científicas y clínicas que respaldan estas aprobaciones.
Un vistazo de esperanza y progreso
La aprobación de estas terapias genéticas marca un hito en la revolución médica. La tecnología CRISPR ha llevado la edición genética a nuevas alturas, ofreciendo tratamientos específicos para enfermedades genéticas devastadoras.
Y es que la innovación en medicina puede abrir las puertas a la esperanza, especialmente para aquellos cuyas vidas se ven afectadas por enfermedades raras y debilitantes.
Este avance no solo representa un logro científico, sino también un rayo de esperanza para el futuro de la medicina y la mejora de la calidad de vida de quienes enfrentan desafíos médicos significativos.
